Tổng hợp định hướng chương Đại cương cứng về chất hóa học hữu cơ
Tài liệu Tổng hợp kim chỉ nan chương Đại cương cứng về hóa học hữu cơ Hoá học tập lớp 11 đã tóm tắt kỹ năng và kiến thức trọng chổ chính giữa về chương Đại cưng cửng về hóa học hữu cơ từ kia giúp học sinh ôn tập để cụ vứng kỹ năng môn Hoá học tập lớp 11.
Bạn đang xem: Ôn tập hóa hữu cơ 11

Lý thuyết mở đầu về hóa học hữu cơ
I. Hợp hóa học hữu cơ với hóa học hữu cơ
1. Khái niệm
- Hợp chất hữu cơ là những hợp hóa học của C trừ oxit của C, muối bột cacbua, muối bột cacbonat, muối hạt xianua.
- Hoá học tập hữu cơ là ngành chất hóa học chuyên nghiên cứu và phân tích các hợp chất hữu cơ.
2. Phân loại hợp chất hữu cơ.
Hợp chất hữu cơ được phân tách thành hidrcacbon và dẫn xuất hidrcacbon.
a/ Hidrcacbon là loại hợp chất hữu cơ đối kháng giản nhất, trong thành phần phân tử chỉ chứa nhì nguyên tố là cacbon và hidro.
- Hidrocacbon mạch hở:
+ Hidrocacbon no: Ankan CH4
+ Hidrocacbon không no có một nối đôi: Anken C2H4
+ Hidrcacbon không no có nhị nối đôi: Ankadien
- Hidrocacbon mạch vòng:
+ Hidrocacbon no: xicloankan
+ Hidrocacbon mạch vòng: Aren
b/ Dẫn xuất của hidrocacbon là những hợp chất mà vào phân tử ngoài C, H ra còn có một số tốt nhiều nguyên tố khác như O, N, S, halogen...
- Dẫn xuất halogen: R – X ( R là gốc hidrocacbon)
- Hợp chất chứa nhóm chức:
- OH - : ancol; - O - : ete; - COOH: axit......
3/ Đặc điểm chung
- Hợp chất hữu cơ duy nhất thiết nên chứa C, hay tất cả H thường gặp gỡ O bên cạnh đó còn có halogen, N, P...
- liên kết chủ yếu trong hợp chất hữu cơ là links cộng hóa trị.
- các hợp chất hữu cơ thường rất dễ bay hơi, dễ dàng cháy, nhát bền nhiệt.
- các phản ứng trong hoá học tập hữu cơ hay chậm, không trả toàn, xảy ra theo không ít hướng thường đề xuất đun rét và gồm xúc tác.
4/ Các cách thức tinh chế hợp chất hữu cơ
- bác bỏ cất: để tách bóc các chất lỏng có ánh nắng mặt trời sôi khác biệt nhiều.
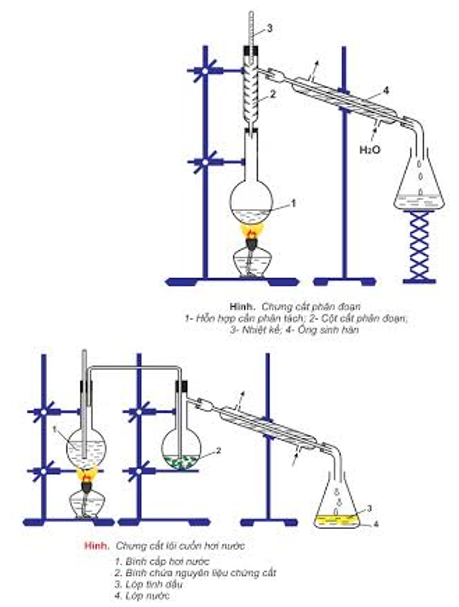
- Chiết: để tách bóc hai chất lỏng không xáo trộn vào nhau.
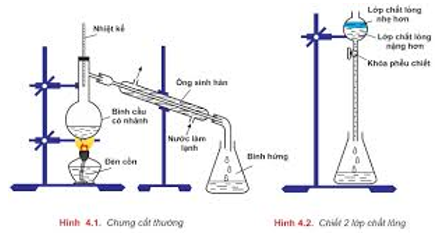
- Kết tinh lại: để tách bóc các hóa học rắn gồm độ tan không giống nhau theo nhiệt độ độ.
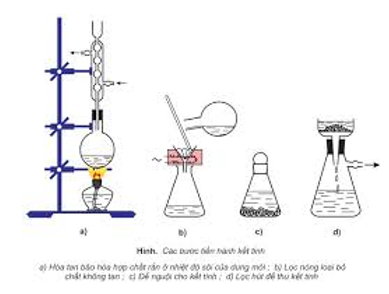
II. So sánh nguyên tố
Để xác định công thức phân tử hợp chất hữu cơ người ta phải xác định :
- Thành phần định tính nguyên tố.
- Thành phần định lượng nguyên tố.
- Xác định khối lượng phân tử.
1. Phân tích định tính nguyên tố.
- Phân tích định tính nguyên tố để xác định thành phần các nguyên tố hóa học chứa trong một chất.
- Muốn xác định thành phần các nguyên tố , người ta chuyển các nguyên tồ vào hợp chất hữu cơ thành các hợp chất vô cơ đối kháng giản rồi nhận ra các sản phẩm đó.
a. Xác định cacbon và hidro.
- Nhận Cacbon: Đốt cháy hợp chất hữu cơ:
C −+O2→ CO2 −+Ca(OH)2→ CaCO3
- Nhận Hidro: Đốt cháy hợp chất hữu cơ:
2H −+O2→ H2O −+CuSO4 khan→ CuSO4.5H2O ( màu xanh lam)
- Hoặc có thể dùng chất hút nước mạnh như : H2SO4 đđ, CaCl2 khan, P2O5.
b. Xác định nitơ và oxi.
- Nhận N: Đốt cháy hợp chất hữu cơ, nếu có mùi khét thì hợp chất đó có nitơ.Hoặc đun hợp chất hữu cơ với H2SO4 đặc ( NaOH đặc) có mùi khai NH3 thì hợp chất đó có chứa nitơ.
CxHyOzNt −+ H2SO4đ, tº→ (NH4)2SO4+......
(NH4)2SO4 + 2NaOH −tº→ Na2SO4 + H2O + NH3↑
- Nhận O : Khó phân tích định tính trực tiếp, thường xác định nhờ định lượng:
mO = mhợp chất – tổng khối lượng các nguyên tố
c. Xác định halogen.
khi đốt cháy hợp chất hữu cơ chứa clo bị phân hủy, clo tách ra dưới dạng HCl, ta dùng dung dịch AgNO3
HCl + AgNO3 → AgCl↓ + HNO3
2. Phân tích định lượng các nguyên tố:
- Phân tích định lượng các nguyên tố xác định khối lượng của mỗi nguyên tố hóa học chứa trong hợp chất hữu cơ.
- Muốn định lượng nguyên tố, người ta chuyển các nguyên tố trong hợp chất hữu cơ thành các hợp chất vô cơ solo giản, định lượng chúng, từ đó suy ra khối lượng từng nguyên tố có vào một chất.
a. Định lượng cacbon và hidro.
VD: Đốt cháy chất hữu cơ A thu được CO2 và H2O và N2
mC (A) = mC(CO2) = nCO2.12
mH(A) = mH(H2O) = nH2O.2
b. Định lượng nitơ
mN(A) = nN2.28
c. Định lượng oxi
mO = m(A) – ( mC + mH + mN ).
* Chú ý :
- Dùng H2SO4 đặc, P2O5, CaCl2 khan hấp thụ H2O.
- Dùng NaOH, KOH, Ca(OH)2 hấp thụ CO2, độ tăng khối lượng của bình tốt khối lượng kết tủa CaCO3 giúp ta tính được CO2
- Chỉ dùng CaO, Ca(OH)2, NaOH hấp thụ sản phẩm gồm CO2 và H2O thì khối lượng bình tăng chính là tổng khối lượng CO2 và H2O.
3. Thành phần nguyên tố:
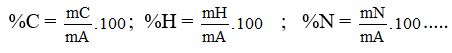
Lý thuyết bí quyết phân tử hợp hóa học hữu cơ
I. Công thức đơn giản nhất
1. Công thức đơn giản và dễ dàng nhất (CTĐGN)
- cho thấy thêm số nguyên tử của các nguyên tố vào phân tử.
cho thấy thêm tỉ lệ đơn giản dễ dàng nhất thân số nguyên tử của các nguyên tố trong phân tử.
Ví dụ: CTĐGN của etilen (CH2)n, của glucozo (CH2O)n (với n là số nguyên dương, chưa xác định).
2. Cách cấu hình thiết lập CTĐGN
hòa hợp chất chứa C, H, O bao gồm dạng CxHyOz.
* Để lập CTĐGN ta lập:
x : y : z = nC : nH : nO
= mC/12 : mH/1 : mO/16
= %(m)C/12 : %(m)H/1 : %(m)O/16
Sau đó đổi khác thành xác suất tối giản.
II. Tùy chỉnh cấu hình công thức phân tử
1. Xác định khối lượng mol phân tử
- Đối với hóa học khí và chất lỏng dễ dàng hóa hơi, fan ta xác định trọng lượng mol phân tử nhờ vào tỉ khối của bọn chúng (ở thể khí) so với chất khí vẫn biết theo công thức:
MA = MB.dA/B; MA = 29.DA/kk
- Đối với chất rắn và chất lỏng khó khăn hóa hơi, bạn ta đo độ tăng ánh sáng sôi của hỗn hợp so cùng với dung môi cùng tính được trọng lượng mol phân tử của chất tan không phai hơi, không hóa học điện li.
2. Tùy chỉnh thiết lập công thức phân tử (CTPT)
cho biết thêm số nguyên tử của mỗi nguyên tố trong một trong những phần tử đúng theo chất.
Ví dụ: CTPT của etilen C2H4, glucozo C6H12O6, benzen C6H6. Liên hệ với CTĐGN sinh sống trên, hệ số n đối với etilen: n = 2, cùng với glucozo n = 6.
* dục tình giữa CTPT với CTĐGN:
- Số nguyên tử của những nguyên tố vào CTPT là số nguyên lần trong CTĐGN.
- trong tương đối nhiều trường hợp, CTĐGN chính là CTPT.
- một số chất có CTPT khác nhau, nhưng bao gồm cùng CTĐGN.
Xem thêm: Bật Mí 3 Cách Làm Nước Chấm Thịt Nướng Hàn Quốc, Ngon Đúng Điệu
* giải pháp lập CTPT hợp chất hữu cơ:
a. Phụ thuộc vào thành phần phần trăm trọng lượng các nguyên tố
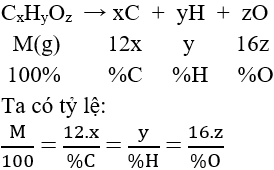
b. Thông qua CTĐGN
trường đoản cú CTĐGN ta bao gồm CTPT là (CTĐGN)n.
Để xác định giá trị n ta dựa vào cân nặng mol phân tử M.
c. Tính thẳng theo khối lượng sản phẩm cháy

Lý thuyết kết cấu phân tử hợp chất hữu cơ
I. Thuyết cấu trúc hóa học
1. Ngôn từ thuyết cấu trúc hóa học
- vào phân tử hợp chất hữu cơ, những nguyên tử links với nhau theo đúng hóa trị cùng theo một vật dụng tự độc nhất định. đồ vật tự liên kết đó gọi là kết cấu hóa học. Sự biến hóa thứ tự link đó, tức là đổi khác cấu sản xuất hóa học, sẽ khởi tạo ra hợp hóa học khác.
Ví dụ: bí quyết phân tử C2H6O gồm hai công thức kết cấu (thứ tự liên kết khác nhau) ứng với 2 hợp chất sau:
H3C−O−CH3: đimetyl ete, chất khí, không công dụng với Na.
H3C−CH2−O−H: ancol etylic, hóa học lỏng, tác dụng với Na giải phóng hiđro.
- vào phân tử hợp hóa học hữu cơ, cacbon gồm hóa trị 4. Nguyên tử cacbon ko những rất có thể liên kết cùng với nguyên tử những nguyên tố khác nhưng còn link với nhau thành mạch cacbon.
Ví dụ:
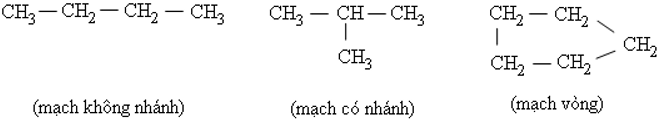
- Tính chất của những chất phụ thuộc vào nhân tố phân tử (bản chất, con số các nguyên tử) và cấu tạo hóa học tập (thứ trường đoản cú liên kết các nguyên tử).
Ví dụ:
- nhờ vào thành phần phân tử: CH4 là chất khí dễ dàng cháy, CCl4 là hóa học lỏng không cháy; CH3Cl là hóa học khí không có tính năng gây mê, còn CHCl3 là chất lỏng có công dụng gây mê.
- Phụ thuộc cấu tạo hóa học: CH3CH2OH và CH3OCH3 khác biệt cả về tính chất hóa học.
2. Đồng đẳng đồng phân
a. Đồng đẳng
- Đồng đẳng là hiện tại tượng những chất cơ học có cấu trúc và đặc thù hóa học tương tự nhau tuy thế thành phần phân tử khác biệt một hay nhiều nhóm CH2.
- các chất thuộc thuộc dãy đồng đẳng vừa lòng thành một hàng đồng đẳng gồm công thức chung.
b. Đồng phân
- Đồng phân là những chất hữu cơ gồm cùng cách làm phân tử nhưng cấu trúc khác nhau nên đặc điểm hóa học khác nhau.
- Cần để ý phân biệt đồng phân kết cấu và đồng phân lập thể (đồng phân cis – trans).
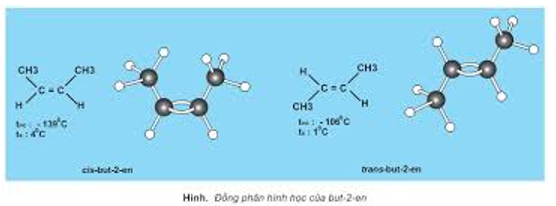
II. Liên kết trong phân tử hợp chất hữu cơ
1. Các loại liên kết trong phân tử hợp hóa học hữu cơ
- link thường gặp mặt trong hợp hóa học hữu cơ là links CHT, gồm link σ và links π.
- Sự tổ hợp của link σ và π chế tạo thành link đôi hoặc ba (liên kết bội).
a. Link đơn (σ)
- do 1 cặp electron chế tác thành, được trình diễn bằng 1 gạch ốp nối thân 2 nguyên tử.
- links σ bền.
b. Links đôi (1 σ và 1 π)
- vị 2 cặp electron chế tạo ra thành, được màn biểu diễn bằng 2 gạch nối giữa 2 nguyên tử.
- tất cả 1σ bền cùng 1 π nhát bền.
c. Links ba (1 σ và 2 π)
- vì 3 cặp electron chế tạo thành, được biểu diễn bằng 3 gạch ốp nối thân 2 nguyên tử.
- tất cả 1σ bền với 2 π yếu bền.
* các liên kết song và cha gọi là links bội.
- lúc nguyên tử cacbon tham gia liên kết đơn, các obitan nguyên tử hóa trị lai hóa loại sp3 (lai hóa tứ diện đều). Góc lai 109’28”.
- lúc nguyên tử cacbon tham gia links đôi, những obitan nguyên tử hóa trị lai hóa kiểu sp2 (lai hóa đều). Góc lai hóa 120º. Ví dụ: Phân tử C2H4.
- khi nguyên tử cacbon tham gia links 3, những obitan nguyên tử hóa trị lai hóa dạng hình sp (lai hóa đường thẳng). Góc lai hóa 180º. Ví dụ: Phân tử C2H2.
2. Những loại phương pháp cấu tạo
cho biết trật trường đoản cú liên kết của các nguyên tử trong phân tử. Khi viết CTCT phải nhất thiết đảm bảo đúng hóa trị của những nguyên tố. Rất có thể viết CTCT bên dưới dạng không thiếu thốn và rút gọn.
- công thức khai triển: biểu diễn trên khía cạnh phẳng giấy tất cả các liên kết giữa các nguyên tử.
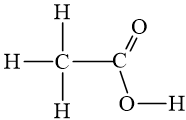
- phương pháp CT thu gọn:
* những nguyên tử hoặc nhóm nguyên tử cùng liên kết với một nguyên tử C được viết thành 1 nhóm.
* Hoặc chỉ biểu diễn liên kết giữa những nguyên tử C và với team chức (mỗi đầu đoạn trực tiếp hoặc điểm gấp khúc là một trong cacbon, không biếu thị số nguyên tử H links với cacbon).
Ví dụ: Viết công thức cấu trúc của axit axetic.
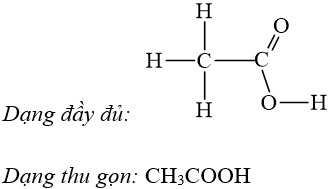
III. Đồng phân cấu tạo
1. định nghĩa đồng phân cấu tạo
Butan−1−ol với đietylete có cùng công thức phân tử C4H10O nhưng mà do không giống nhau về cấu tạo hóa học tập nên không giống nhau về đặc thù vật lí và đặc thù hóa học.
Vậy phần nhiều hợp chất bao gồm cùng công thức phân tử nhưng mà có cấu tạo hóa học khác biệt gọi là mọi đồng phân cấu tạo.
2. Phân nhiều loại đồng phân cấu tạo
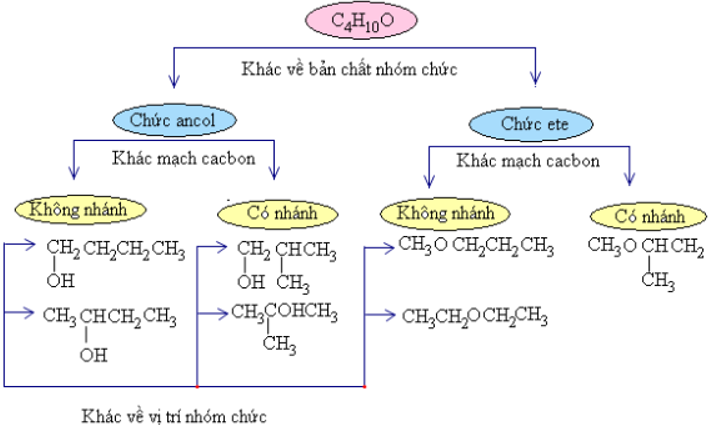
mọi đồng phân khác biệt về bản chất nhóm chức điện thoại tư vấn là đồng phân nhóm chức. đông đảo đồng phân khác biệt về sự phân nhánh mạch cacbon call là đồng phân mạch cacbon. Gần như đồng phân không giống nhau về địa điểm nhóm chức điện thoại tư vấn là đồng phân địa điểm nhóm chức.
IV. Phương pháp biểu diễn cấu trúc không gian phân tử hữu cơ
1. Công thức phối cảnh
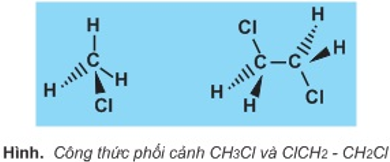
công thức phối cảnh là một trong những loại phương pháp lập thể.
Đường nét tức thì biểu diễn links nằm cùng bề mặt trang giấy.
Đường đường nét đậm màn trình diễn liên kết nhắm tới mắt ta (ra vùng trước trang giấy).
Đường đường nét đứt biểu diễn link hướng ra xa đôi mắt ta (ra vùng phía đằng sau trang giấy).
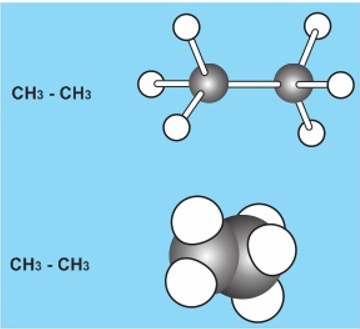
2. Quy mô phân tử
a. Mô hình rỗng
các quả mong tượng trưng cho những nguyên tử, các thanh nối tượng trưng cho những liên kết thân chúng. Góc thân hai các thanh nối bằng góc lai hóa.
b. Quy mô đặc
các quả cầu cắt vát tượng trưng cho các nguyên tử được ghép cùng với nhau theo như đúng vị trí không khí của chúng.
V. Đồng phân lập thể
1. Tư tưởng về đồng phân lập thể
- Ứng với công thức kết cấu CHCl=CHCl tất cả hai cách bố trí không gian không giống nhau dẫn tới hai chất đồng phân:
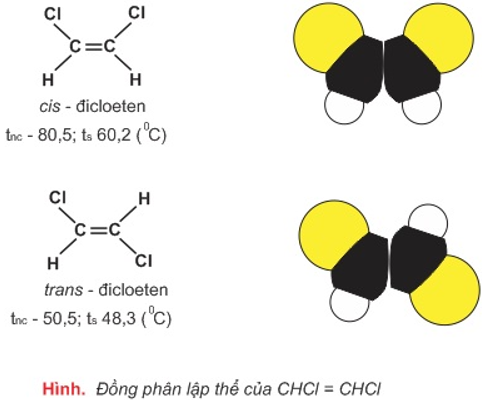
- Kết luận:
- Đồng phân lập thể là hầu hết đồng phân có cấu trúc hóa học tập như sau (cùng bí quyết cấu tạo) nhưng không giống nhau về sự phân bố không khí của những nguyên tử trong phân tử (tức khác nhau về kết cấu không gian của phân tử).
2. Quan hệ tình dục giữa đồng phân cấu tạo và đồng phân lập thể
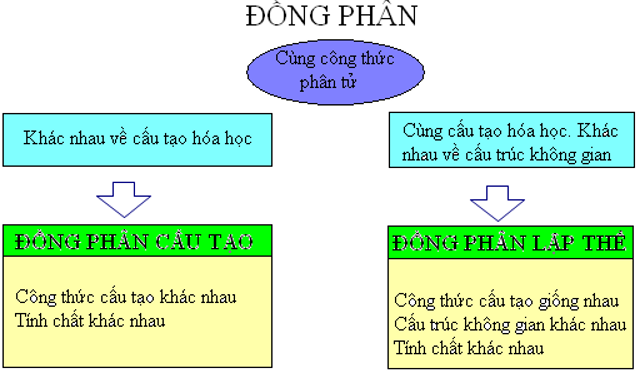
3. Cấu trúc hóa học tập và cấu trúc hóa học
- Cấu tạo hóa học cho ta biết các nguyên tử link với nhau theo máy tự nào, bằng links đơn hay link bội, mà lại không cho thấy sự phân bổ trong không khí của chúng. Cấu trúc hóa học tập được biểu diễn bởi phương pháp cấu tạo.
- cấu trúc hóa học tập và cấu tạo không gian của phân tử vừa lòng thành cấu trúc hóa học.
- cấu trúc hóa học vừa mang lại biết cấu tạo hóa học vừa cho thấy thêm sự phân bổ trong không khí của các nguyên tử vào phân tử. Kết cấu hóa học hay được biểu diễn bởi công thức lập thể.










